僉僩僒儞偲偦偺壔妛廋忺懱偺暘愅壔妛傊偺棙梡
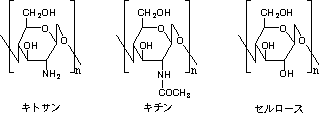
丂僉僩僒儞偼僌儖僐僒儈儞偑兝-1,4 寢崌偱廳崌偟偨揤慠偺傾儈僲懡摐偱偡丅偙偺暔幙偼僄價丒僇僯偺峛梾偵懚嵼偡傞僉僠儞傪扙傾僙僠儖壔偡傞偙偲偱摼傜傟傑偡丅僉僠儞偲僉僩僒儞偺堘偄偵偮偄偰尩枾側掕媊偼偁傝傑偣傫偑丄堦斒偵扙傾僙僠儖壔棪偑栺80亾埲忋偺傕偺傪僉僩僒儞偲屇傫偱偄傑偡丅僉僩僒儞偼僙儖儘乕僗偵師偖僶僀僆儅僗偱丄偦偺峔憿傕椶帡偟偰偄傑偡偑丄僙儖儘乕僗偵斾妑偡傞偲嶻嬈揑側棙梡偼傑偩敪揥搑忋偵偁傝傑偡丅
丂丂丂丂
丂僉僩僒儞偼偦偺峔憿偐傜梊憐偝傟傞傛偆偵丄斀墳惈偺崅偄俀埵偺傾儈僲婎傪夘偟偰偝傑偞傑側廋忺懱偵桿摫偡傞偙偲偑弌棃傑偡丅変乆偼僉僩僒儞傪壔妛廋忺偟偰尦棃僉僩僒儞偺桳偡傞婡擻傗摿惈傪傛傝崅搙壔偟丄暘愅壔妛揑側棙梡傪恾偭偰偄傑偡丅
丂椺偊偽僒儕僠儖傾儖僨僸僪偲偺斀墳偱惗偠偨僔僢僼墫婎傪娨尦偡傞偲2-僸僪儘僉僔儀儞僕儖僉僩僒儞乮俫俛俠乯偑崌惉偱偒丄俫俛俠偱廋忺偟偨僌儔僢僔乕僇乕儃儞揹嬌傪梡偄偰俠倁朄偵傛傝摵偲墧僀僆儞傪慖戰揑偵暘愅偡傞偙偲偑弌棃傑偡丅傑偨丄僺儕僪僉僒乕儖椶帡懱偱廋忺偟偨僉僩僒儞傪姶墳晹偵帩偮岝僼傽僀僶僙儞僒偼垷墧僀僆儞偵懳偟偰寀岝惈偺墳摎傪帵偟傑偡丅
丂僉僩僒儞乛億儕價僯乕儖傾儖僐乕儖傪僋儔僢僪偲偡傞撪晹慡斀幩宆偺岝僼傽僀僶僙儞僒偼僋儔僢僪偺孅愜棪曄壔傪棙梡偟偨傕偺偱偡偑丄悈拞偺桳婡梟攠偵墳摎傪帵偟丄摿偵庰椶拞偺僄僞僲乕儖偺儕傾儖僞僀儉側掕検傊偺棙梡偑婜懸偱偒傑偡丅傑偨丄僋儔僢僪傪怓慺偱廋忺偡傞偙偲偱桳婡巁偵懳偡傞慖戰惈傪崅傔偨僙儞僒傪峔抸偱偒傑偡丅
丂堦曽丄僔僋儘僨僉僗僩儕儞傪暘巬偝偣偨僉僩僒儞傪屌掕憡偲偡傞俫俹俴俠偱偼丄傾儈僲巁桿摫懱偵懳偟偰丄捠忢偺僔僋儘僨僉僗僩儕儞屌掕憡偺応崌偲堎側傞僉儔儖暘棧嫇摦偑尒傜傟傑偡丅摨條偵俫俹俴俠僉儔儖暘棧傊偺棙梡椺偲偟偰丄攝埵巕岎姺儌乕僪傪敪尰偡傞屌掕憡傪嫇偘傞偙偲偑弌棃傑偡丅偙偺屌掕憡偵梡偄傞桿摫懱偼丄僉僩僒儞崪奿偵怴偨側傾儈僲巁攝埵巕晹埵傪桳偟丄僉僩僒儞偲兛-働僩巁偲偱惗惉偟偨僔僢僼墫婎傪娨尦偡傞偲摼傜傟傑偡丅
尰嵼偼丄僝儖僎儖朄傪梡偄偰僉僩僒儞廋忺懱傪僔儕僇僎儖儅僩儕僢僋僗拞偵曪妵偝偣偨俫俹俴俠屌掕憡偺挷惢偍傛傃丄僔儕僇僎儖晹埵偵壔妛廋忺偱偝傜偵婡擻傪帩偨偣傞偙偲偱丄曪妵億儕儅乕偲廋忺僔儕僇僎儖晹埵偺俀廳擣幆応傪桳偡傞屌掕憡偺奐敪傪峴偭偰偄傑偡丅
俫俛俠偱廋忺偟偨僌儔僢僔乕僇乕儃儞揹嬌
A Glassy Carbon Electrode Modified with N-(2-Hydroxybenzyl)chitosan for voltammetric Determinations of Cu2+ and Pb2+
(Y. Kurauchi, E. Tsurumori, K. Ohga, Bull. Chem. Soc. Jpn., 62, 1341 (1989).
僺儕僪僉僒乕儖椶帡懱偱廋忺偟偨僉僩僒儞傪姶墳晹偵帩偮岝僼傽僀僶僙儞僒
Fluorometric Determination of Zn2+, Cd2+ and Ga3+ Ions with a Fiber-Optic Sensor Having a Pyridoxal Isomer-Modified Chitosan/Agarose Gel as a Sensing Probe
(Y. Kurauchi, R. Hayashi, N. Egashira and K. Ohga, Anal. Sci.,
8, 837(1992))
僉僩僒儞乛億儕價僯乕儖傾儖僐乕儖傪僋儔僢僪偲偡傞撪晹慡斀幩宆偺岝僼傽僀僶僙儞僒
Fiber-optic Sensor with a Chitosan/Poly(vinyl alcohol) Cladding for the Determination of Ethanol in Alcoholic Beverages
(Y. Kurauchi, T. Yanai, N. Egashira and K. Ohga, Anal. Sci., 10,
213(1994))
桳婡巁偵懳偡傞慖戰惈傪崅傔偨僙儞僒
Fiber-optic Sensor with a Dye-Modified Chitosan/Poly(vinyl alcohol) Cladding for the Determination of Organic Acids
(Y. Kurauchi, T. Ogata, N. Egashira and K. Ohga, Anal. Sci., 12,
55(1996))
僔僋儘僨僉僗僩儕儞傪暘巬偝偣偨僉僩僒儞傪屌掕憡偲偡傞俫俹俴俠
Preparation of a b-Cyclodextrin-Modified N-Carboxymethylchitosan and its Chromatographic Behavior as a Chiral HPLC Stationary Phase
(Y. Kurauchi, H.Ono, B.Wang, N. Egashira and K. Ohga, Anal. Sci., 13, 47 (1997))